Pelo menos três dos 11 membros independentes do comité que votaram unanimemente contra a recomendação do medicamento renunciaram posteriormente, e um relatório do Congresso dos EUA afirmou, após uma investigação, que a aprovação acelerada estava “cheia de irregularidades”. Em resposta às críticas, Christopher Viehbacher, presidente e CEO da Biogen, afirmou que o Aduhelm foi uma descoberta inovadora que abriu caminho para uma nova classe de medicamentos e revitalizou os investimentos nessa área.
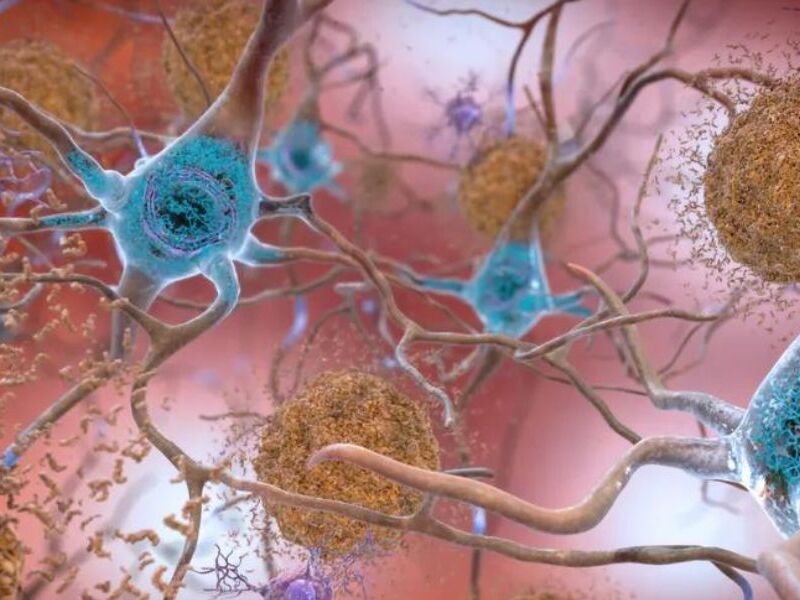
O Aduhelm, um anticorpo monoclonal que busca reduzir o acúmulo de uma proteína chamada beta-amiloide no tecido cerebral, considerado a causa do Alzheimer, foi testado em dois estudos em humanos em estágio avançado. A droga mostrou redução do comprometimento cognitivo em um dos estudos, mas não no outro. O relatório do Congresso de dezembro de 2022 apontou que a FDA “considerou o Aduhelm sob o caminho de aprovação tradicional usado para a maioria dos medicamentos por nove meses, antes de mudar abruptamente o curso e conceder a aprovação sob a via rápida após um “período de revisão de três semanas”.
Além disso, o relatório legislativo afirmou que a FDA e a Biogen também “colaboraram inapropriadamente” para um documento informativo conjunto para um comitê consultivo importante. “O processo de aprovação da FDA estava repleto de irregularidades”, consta no relatório. Em meio a toda a polêmica em torno do Aduhelm, a empresa Biogen optou por retirar o medicamento do mercado, visando concentrar esforços e recursos no desenvolvimento do Leqembi.